欧洲市场
欧洲市场对于口罩的管理分为两个主要类别,个人防护口罩和医用口罩。个人防护口罩主要是工业用防护,医用口罩主要是医院使用。
医用口罩

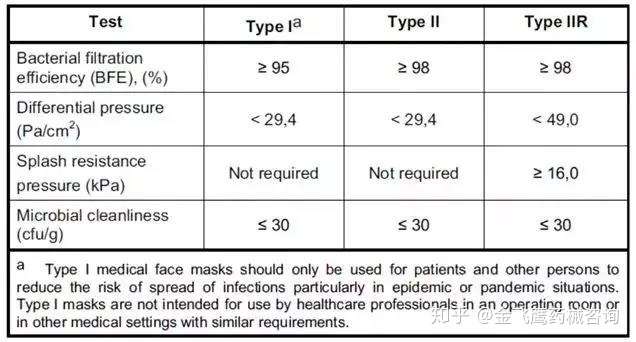 欧洲医用外科口罩的分类
欧洲医用外科口罩的分类
1.非无菌方式提供
1)编制技术文件
2)提供测试报告(可以提供熔喷布性能测试报告和无纺布的生物学报告)
3)编制DOC
4)指定欧盟代办代表并完成欧洲注册
2.无菌方式提供
1)灭菌验证
2)建立ISO13485体系
3)编制技术文件
4)提供测试报告(口罩本身的生物学、性能、无菌等测试报告)
5)公告机构审核(目前只能按照MDR审核,预计近期没有NB可以审核)
6)获CE证书
7)指定欧盟代办代表并完成欧洲注册

防护口罩
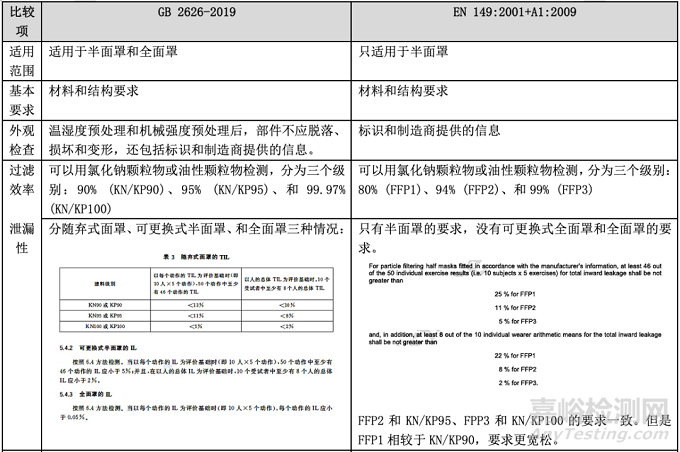
防护口罩的欧洲标准是EN149,按照标准将口罩分为FFP1/FFP2和FFP3三个类别,具体的指标见下图。
 欧洲防护口罩分类
欧洲防护口罩分类
美国法规对医用口罩和工业防护口罩同样是区分管理,其中医用口罩由FDA管控,而防护口罩则由NIOSH管控。大家熟知的N95口罩就来源于NIOSH对口罩分类中的一个类别。
美国对于医用口罩的管理机构是FDA,在FDA系统中对于口罩的分类代码有如下3个。其中一个是外科口罩,一个是儿科口罩,一个是带有抗菌/抗病毒介质的外科口罩,见下图。
 美国FDA分类数据库中的口罩
美国FDA分类数据库中的口罩

(1)已经获得NIOSH批准的N95口罩可以直接注册
 878.4040的释义
878.4040的释义
从上图可以看出,如果你的N95口罩获得了NIOSH的批准,生物学测试、阻燃测试和血液穿透测试都通过了,那么你是可以豁免510K的,可以直接进行工厂注册和器械列名。
(2)获得持有510K的制造商的代办,作为其代工厂使用其510K批准号进行企业注册和器械列名。
申请方需要获得代办书,需要签署正式的质量协议,FDA会进行核实和抽查。如果使用未经许可的号码,将会导致产品召回的风险。

NIOSH的口罩防护等级认证程序复杂,包括:

澳洲市场

 TGA注册书
TGA注册书
加拿大
加拿大医疗器械产品分为4类,其中1类风险低,不需要做器械注册(MDL),只需要进行MDEL(制造商注册),见下图。
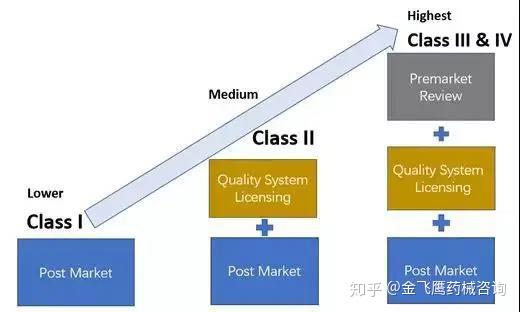 加拿大医疗器械管理示意图
加拿大医疗器械管理示意图









评论前必须登录!
注册