口罩检测
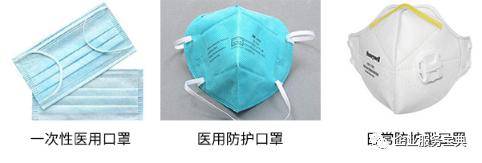
随着新型冠状病毒肺炎的蔓延,口罩等医疗防护用品成为日常必需品,为健康安全构建起关键的防线。口罩分为一次性医用口罩、医用防护口罩、PM2.5防护口罩、日常防护型口罩等。
口罩类别
随着新型冠状病毒肺炎的蔓延,口罩等医疗防护用品成为日常必需品,为健康安全构建起关键的防线。口罩分为一次性医用口罩、医用防护口罩、PM2.5防护口罩、日常防护型口罩等。
申请流程
填写申请表
寄样品到检测机构
实验室安排样品测试
测试通过后,出测试报告
国内销售
测试产品
一次性使用医用口罩、医用外科口罩、日常防护型口罩。
主要测试项目
外观、耐摩擦色牢度、甲醛含量、pH值、可分解芳香胺致癌染料、口罩带及口罩带与口罩体的连接处断裂能力、呼吸阀盖牢处、大肠菌群、绿脓杆菌、金刘色葡萄球菌、溶血性链球菌、真菌菌落总数、细菌菌落总数、环氧乙烷残留量、包装与标识。
测试标准
YY/T 一次性使用医用口罩执行标准 GB/T 日常防护型口罩技术规范
GB 《医用防护口罩技术要求》
YY 《医用外科口罩》
YY/T 《一次性使用医用口罩》
GB/T 《呼吸防护用品自吸过滤式防颗粒物呼吸器》
GB/T 《日常防护型口罩技术规范》
出口欧洲
测试产品
个人防护口罩 、医用口罩
性能测试、生物学测试、呼气阻力、呼气阀泄露、过滤效率等。
标准依据
医用口罩:EN14683标准,按欧盟医疗器械指令93/42/EEC(MDD)或欧盟医疗器械条例EU2017/745(MDR)加贴CE标志。
(1)无菌医用口罩:必须由代办公告机构进行CE认证。
(2)非无菌医用口罩:企业只需进行CE自我符合性声明,不需要通过公告机构认证。在准备好相应文件及测试报告等资料后,即可自行完成符合性声明。
个人防护口罩:EN149标准,需要符合欧盟个人防护设备条例EU2016/425(PPE)要求,由代办公告机构进行CE认证并颁发证书。
出口美国
测试产品
个人防护口罩
医用口罩
个人防护口罩:由美国国家职业安全卫生研究所(NIOSH)管理。
医用口罩:由美国食品药品监督管理局(FDA)管理
医用口罩需通过FDA注册,企业直接向FDA申请并提交相关材料。此外还有两种可选途径:
(1)已经获得NIOSH注册的N95口罩,在产品生物学测试、阻燃测试和血液穿透测试通过的情况下,可以豁免产品上市登记(510K),直接进行FDA工厂注册和医疗器械列名。
(2)如果获得持有510K的制造商的代办,可以作为其代工厂使用其510K批准号进行企业注册和器械列名。
防护口罩需通过NIOSH注册,企业直接在NIOSH申请。















评论前必须登录!
注册